a Genel Cerrahi ve Klinik Beslenme Anabilim Dalı, Varşova Tıp Üniversitesi, Varşova, Polonya
b Pirogow Hastanesi, Klinik Beslenme Merkezi, Lodz, Polonya
c İmmünopatoloji Anabilim Dalı, Varşova Tıp Üniversitesi, Varşova, Polonya
d İnsan Gelişimi ve Sağlık Akademi Birimi, Tıp Fakültesi, Southampton Üniversitesi, Southampton, Birleşik Krallık
e NIHR Southampton Biyomedikal Araştırma Merkezi, Southampton Üniversite Hastanesi NHS Vakfı, Southampton Üniversitesi, Southampton, Birleşik Krallık
article info
Article history:
Received 18 January 2018
Accepted 27 May 2018
Keywords:
Intestinal failure
Home parenteral nutrition
Lipid emulsion
Fatty acid
Inflammation
Essential fatty acid deficiency
Corresponding author.
E-mail address: [email protected] (S. Osowska).
Contents lists available at ScienceDirect
Clinical Nutrition
journal homepage: http://www.elsevier.com/locate/clnu
https://doi.org/10.1016/j.clnu.2018.05.028
0261-5614/© 2018 Published by Elsevier Ltd.
Evde Parenteral Beslenen Yetişkinlerde Lipid Bileşenleri Değişiminin Etkisi [Çeviri]
ÖZET
Giriş ve Amaç: Evde PN tedavisi alan hastaların (erişkin), parenteral nütrisyon (PN) rejiminde kullandığı farklı lipid emülsiyonlarının (LE’ler) serum lipid düzeylerine etkisi henüz tam olarak açıklanmamıştır. Bu çalışmada; HPN (Evde Parenteral Nütrisyon) alan yetişkin hastalarda, soya yağı bazlı bir LE (Intralipid) ‘nin yerine, balık yağı içeren (n-3 sağlayan) lipid emülsiyonlarının (SMOFLipid) ve zeytin yağı bazlı lipid emülsiyonlarının (ClinOleic) kullanımının etkisi araştırıldı.
Yöntemler: LE olarak Intralipid ile uzun süreli HPN alan otuz iki yetişkin, 60 gün boyunca SMOFLipid (13 kişi) veya ClinOleic (19 kişi) almak üzere iki ayrı gruba transfer edildi. Karaciğer fonksiyon belirteçleri, kolesterol, trigliseritler, total yağ asidi profili ve birkaç sitokin çalışmanın başlangıcında ve 60 gün sonrasında ölçüldü.
Bulgular: SMOFLipid; karaciğer fonksiyon belirteçlerini, kan lipitlerini veya plazma sitokinlerini etkilemedi. ClinOleic hem gama glutamil transpeptidase (P= 0.044) hem de interlökin-8 (P =0.030) konsantrasyonlarını düşürdü. Her iki LE de plazmanın yağ asidi profilinde belirgin değişiklikler meydana getirmiştir. SMOFLipid; linoleik asit, bazı n-6 yağ asitleri ve esansiyel yağ asidi (EFA) oranlarında önemli düşüşler meydana getirmiş ve n-3 yağ asitlerinden eikosapentaenoik asit ve doksaheksaenoik asit oranlarında önemli artışlar sağlamıştır. ClinOleic; bazı doymuş yağ asitleri, linoleik asit, birkaç n-6 yağ asidi, tüm n-3 yağ asitleri ve mead asidi (Mead asidi bir omega-9 yağ asididir. Kanda yüksek miktarda bulunması, esansiyel yağ asidi (EFA) eksikliğinin bir göstergesidir. Mead asidi kıkırdakta büyük miktarlarda bulunur.) oranlarında önemli düşüşler ve oleik asit oranında önemli bir artış göstermiştir. SMOFLipid veya ClinOleic plazmada mead’in araşidonik aside oranını değiştirmedi. Hiçbir hastada, EFA eksikliğini belirtmek için kullanılan > 0.2 mead asit/araşidonik asit oranı yoktu.
Sonuç: Daha önce Intralipid kullanan yetişkin HPN kullanan hastalarda hem SMOFLipid hem de ClinOleic, plazmanın yağ asidi profilini önemli ölçüde değiştirir. Her iki LE’de bu hastalarda EFA eksikliğini tetiklememektedir. SMOFLipid karaciğer fonksiyon belirteçlerini veya iltihabını değiştirmedi. Buna karşılık ClinOleic; hepsi olmasa da bazı karaciğer fonksiyon ve inflamasyon belirteçlerini azalttı. SMOFLipid ve ClinOleic, yetişkin HPN hastalarında kullanım için düşünülebilir.
1. GİRİŞ
Evde parenteral beslenme (HPN), uzun süreli gastrointestinal sistem yetmezliği nedeniyle uzun süreli parenteral beslenme (PN) öngörülen hastalarda yetersiz beslenmeyi önlemek için yeterli miktarda amino asit, glikoz, lipid, elektrolit ve su sağlamayı amaçlayan köklü-yerleşik bir tedavi yöntemidir [1-3]. HPN’deki geleneksel lipit kaynağı, emülsifiye edilmiş soya fasulyesi yağıdır. Soya yağı, içerdiği yağ asitlerinin yaklaşık %50’sini oluşturan n-6 çoklu doymamış yağ asidi (PUFA) linoleik asit (18: 2n-6) bakımından zengindir [4]. Linoleik asit, esansiyel bir yağ asididir (EFA). Soya fasulyesi yağının yaklaşık %7’sini (n-3 PUFA) α-linolenik asit oluşturmaktadır (18: 3n-3). Alfa-linolenik asit de esansiyel bir yağ asididir [4]. Bu nedenle, soya fasulyesi yağı iyi bir EFA kaynağıdır. Ancak, soya yağının, yüksek linoleik asit içermesi ya da yüksek fitosterol içermesi nedeniyle karaciğer hastalığı riskini arttırdığı düşünülmektedir (Bağırsak yetmezliği ile bağlantılı karaciğer hastalığı) [5]. Linoleik ve α -linolenik asitler daha uzun zincire, daha fazla doymamış biyoaktif türevlere metabolize edilir. Sırasıyla: Linoleik asit araşidonik aside (20: 4n-6) ve α -linolenik asit eikosapentaenoik aside (EPA; 20: 5n-3) dönüşür. EPA, ayrıca dokosaheksanoik aside metabolize edilebilir (DHA; 22: 6n 3), fakat bu dönüşümün insanlarda sınırlı olduğu düşünülmektedir [6]. Araşidonik asit, EPA ve DHA’nın birçok fizyolojik rolü vardır. Diğerlerinin yanı sıra karaciğer metabolizmasını, kan lipid konsantrasyonlarını, iltihaplanmayı, bağışıklık tepkilerini, kalp fonksiyonlarını ve kan pıhtılaşmasını kontrol ederler [7]. Genel olarak araşidonik asit ve iki n-3 PUFA (EPA ve DHA) birbirine zıt olarak hareket eder. Bu durum genel olarak inflamasyon durumunda; araşidonik asidin pro-enflamatuar rol üstlendiği, EPA ve DHA’nın anti-enflamatuar rol üstlendiği şeklinde açıklanabilir [8-9]. Soya fasulyesi yağının, linoleik asitten zengin olması sebebiyle, araşidonik asidin sentezi için substrat temin ederek iltihaplanmayı teşvik edebileceği ileri sürülmüştür; ayrıca linoleik asidin kendisi, pro-enflamatuar kimyasal mediatörlere yol açmaktadır [10]. Bu nedenle, parenteral beslenmede kullanım için soya yağı içeriği azaltılmış lipit emülsiyonları geliştirilmiştir [4,11].
ClinOleic (Baxter Healthcare), 80:20 (hacim / hacim) zeytinyağı ve soya fasulyesi yağı karışımıdır. Linoleik asit içeriği, yağ asitlerinin yaklaşık %20’sidir ve karışımda en çok bulunan yağ asidi, yaklaşık %60 ile oleik asittir (18: 1n-9). ClinOleic’te yağ asitlerinin yaklaşık %3’ü α -Linolenik asittir [4]. SMOFLipid (Fresenius Kabi), 30: 30: 25: 15 (hacim / hacim / hacim / hacim) soya fasulyesi yağı, orta zincirli trigliserit bakımından zengin yağ, zeytinyağı ve balık yağı karışımıdır. Balık yağı EPA ve DHA kaynağıdır. Linoleik ve α -linolenik asitler, sırasıyla SMOFLipid’de yaklaşık %20 ila %2 oranında bulunurken, EPA ve DHA birlikte yaklaşık %5 oranında bulunur [4]. Bu nedenle hem ClinOleic hem de SMOFLipid, soya fasulyesi yağıyla karşılaştırıldığında az linoleik asit içeriğine sahiptir. Böylece çok fazla n-6 PUFA’nın zararlı sonuçlarından kaçınabilirler [4]. Ayrıca, SMOFLipid sağlığı destekleyici uzun zincirli n-3 PUFA’lar olan EPA ve DHA’yı içerir. Bu nedenle, hem ClinOleic hem de SMOFLipid, HPN hastalarında faydalı olabilir. Buna karşın, bu yeni lipit emülsiyonları ile daha sınırlı linoleik ve α -linolenik asit temininin EFA eksikliğine yol açabileceği endişesi vardır. EFA eksikliğinin biyokimyasal işareti, metabolizma için yetersiz EFA’lar mevcut olduğunda, oleik asitten üretilen mead asidinin (20: 3n-9) artmasıdır [12]. Çoğu zaman bu, mead asidinin araşidonik aside oranı olarak ifade edilir [13].
Birçok ülkede ClinOleic ve SMOFLipid’in birkaç yıldır var olmasına rağmen, evde bakım ortamında yetişkin hastalarda kullanımları konusunda sınırlı sayıda veri vardır ve birebir karşılaştırmalar çok azdır [14]. Bu nedenle; bu çalışmada, yetişkinler tarafından uzun süreli HPN’de kullanılan lipit emülsiyonunun, soya yağı bazlı Intralipid’den (Fresenius Kabi), ClinOleic veya SMOFLipid’e değiştirilmesi sonrası lipid seviyeleri üzerine etkisi karşılaştırılmıştır. 60 gün süren müdahale sonrası karaciğer fonksiyon belirteçleri, kan lipitleri, EFA eksikliği belirteci dahil olmak üzere yağ asitleri ve inflamasyonla ilişkili sonuçlar değerlendirildi.
2. MATERYAL VE METOD
2.1. Çalışma tasarımı ve hasta popülasyonu
Polonya’da iki parenteral beslenme merkezinde (Varşova ve Lodz) Ocak 2016-Eylül 2016 tarihleri arasında gerçekleştirilen, 2 paralel grupla yapılan prospektif (ileriye dönük) ve karşılaştırmalı bir çalışmaydı. Çalışma protokolü ve aydınlatılmış onam formu, Varşova Tıp Üniversitesi Biyoetik Komitesi tarafından onaylandı. Tüm katılımcılardan yazılı hasta onamı alındı. Çalışmaya HPN (19 kadın ve 13 erkek; ort. yaş 58) destekli bağırsak yetmezliği olan 32 erişkin hasta alındı.
Dahil olma kriterleri şunlardı:
- Çalışmaya başlamadan en az 2 yıl öncesinden HPN desteği alıyor olması,
- Haftada 7 kez PN infüzyonu,
- Hastanenin HPN programının bir parçası olması,
- Çalışmaya dahil edilmeden önceki 2 ay boyunca oral beslenme ve ilaç tedavisinin değişmemiş olması.
Çalışmadan dışlanma kriterleri:
- Aktif enfeksiyon veya;
- Karaciğer yetmezliği veya;
- Böbrek yetmezliği veya;
- Hem karaciğer hem böbrek yetmezliği olması.
Tüm hastalar çalışmaya başlamadan önce PN desteklerinin bir parçası olarak Intralipid %20 (Fresenius Kabi, Bad Homburg, Almanya) alıyordu. Bu, Varşova’daki 13 hasta için SMOFLipid %20 (Fresenius Kabi, Bad Homburg, Almanya) ve Łodz’daki 19 hasta için ClinOleic %20 (Baxter SAS, Maurepas-Cedex, Fransa) olarak değiştirildi. Hastalara, lipit emülsiyonunun değişmesinden önce ve sonra aynı miktarda lipit verildi. Kan örnekleri, lipid emülsiyonunun değiştirilmesinden 7 gün önce ve 60 gün sonra toplandı. Bu iki zaman noktası tSTART (başlangıç) ve tEND (sonuç) olarak adlandırıldı.
2.2. Kan işlemleri ve yapılan analizlere genel bakış
Kan pıhtılaşmasını önleyici olarak disodyum-EDTA kullanıldı. Rutin biyokimyasal analizlerin bir kısımı kullanılmıştır.
Aşağıdakiler ölçüldü:
- Total bilirubin,
- Alanin aminotransferaz (ALT),
- Aspartat aminotransferaz (AST),
- Gama glutamiltranspeptidaz (GGT),
- Total kolesterol
- Total trigliseritler
Her iki bölge de bu analizler için aynı metodolojileri kullanmış, ancak normal aralıklar için iki bölgede de farklı aralıklar kullanılmıştır. Bir miktar kan hemen santrifüj edildi ve plazma izole edildi; Bunlar, analize edilinceye kadar -80 ° C’de depolandı.
Aşağıdakiler ölçüldü plazma:
- İnterlökin (IL) -6,
- IL-8,
- IL-10 ve
- Tümör nekroz faktörü (TNF)- α
- Total plazma ve Plazma fosfatidilkolin (PC) ‘deki yağ asitleri.
2.3. Plazma ve plazma PC’de yağ asitlerinin ölçümü
Lipit, antioksidan olarak 0.2 M bütillenmiş hidroksitolüen içeren 5 ml kloroform: metanol (2: 1; hacim / hacim) kullanılarak plazmadan ekstrakte edildi. Sodyum klorür (İM; 1 mL) eklendi ve numune vortekslenip santrifüjlendi. Çözücü faz aspire edildi ve 40 ° C’de kuruyana kadar azot altında buharlaştırıldı. Toplam lipit özü, ikiye bölündü; bir kısmı, toplam plazma lipidindeki yağ asitlerinin analizi için tutuldu ve diğer yarısı, plazma PC’sindeki yağ asitlerinin analizi için kullanıldı. Son olarak, NH2 kartuşlarında (Agilent) katı faz ekstraksiyonu kullanılarak plazma lipit ekstraktından izole edildi. PC, kloroform: metanol (60: 40v / v) içeren kartuşlardan elüe edildi ve 40 ° C’de kuruyana kadar azot altında buharlaştırıldı. Hem toplam lipit özü hem de PC için, yağ asitleri çıkarıldı ve eş zamanlı olarak, yağ asidi metil esterlerini oluşturmak üzere en az 2 saat boyunca 50 ° C’de en az 2 saat boyunca metanol içerisinde 1 mL %2 H2S04 (hacim / hacim) ile inkübe edilerek metil esterlere türevlendirildi. Numuneler daha sonra nötrleştirildi ve yağ asidi metil esterleri, gaz kromatografısi ile analiz için heksan içine aktarıldı. Yağ asidi metil esterleri, bir alev iyonizasyon detektörü ile donatılmış HP6890 gaz kromatografisindeki bir BPX-70 kaynaşık silika kılcal kolonunda (30 m 0.2 mm 0.25 mm, SGE tarafından imal edildi) ayrıldı. Gaz kromatografi çalışma koşulları, başka yerlerde tarif edildiği gibidir [15]. Kalibrasyon referans standardı olarak bir Supelco® 37 Komponent FAME Mix kullanıldı (Sigmae-Aldrich, Irvine, UK). Hem toplam plazma hem de PC için yağ asidi verileri, mevcut toplam yağ asitlerinin yüzdesi olarak ifade edilir.
2.4. Plazma sitokin konsantrasyonlarının ölçümü
Plazmada TNF- α, IL-1 β, IL-6, IL-8, IL-10, IL-12 ve interferon (IFN) – γ konsantrasyonları, yüksek hassasiyetli bir Bio-Techne multiplex immunoassay kullanılarak ölçüldü (R&D Systems Abingdon, İngiltere). Kullanımdan önce reaktifler oda sıcaklığına getirildi ve üreticinin talimatlarına göre kullanımdan hemen önce dilüsyonlar hazırlandı. Örnekler, bir Bio Radplex Luminex Analyzer kullanılarak okundu. Veriler pg / ml plazma olarak ifade edildi.
2.5. İstatistiksel analiz
Veriler Kolmogorove-Smirnov testi (Bir örneklemin dağılımının düzgün dağılıp dağılmadığını, güvenilirliğini sınayan testtir) kullanılarak normallik açısından kontrol edildi. Verilerin çoğu çarpıktı ve bu nedenle tüm veriler medyan ve çeyrekler arası aralıkla ifade edildi.
Tedavi grupları arasında tEND (sonuç) grubundakiler için ManneWhitney U testi kullanılarak karşılaştırmalar yapıldı. (Mann-Whitney U testi niceliksel ölçekli gözlemleri verilen iki örneklemin aynı dağılımdan gelip gelmediğini incelemek kullanılan bir parametrik olmayan istatistik testtir.) Tedavi grubu içerisinde tEND (sonuç) ile tSTART (başlangıç) arasında karşılaştırmalar Wilcoxon işaretli sıralar testi ile yapılmıştır. (Tekrarlı ölçümler ile kullanılmak için tasarlanmıştır; yani katılımcılar iki durum üzerinden değerlendirildiğinde ya da iki farklı durum altında değerlendirildiğinde kullanılır.) İstatistiksel analizler SPSS 21 sürümü kullanılarak yapıldı. Tüm durumlarda, istatistiksel olarak anlamlı bir farkı olduğunu belirtmek için P <0,05 değeri alındı.
3. BULGULAR
3.1. Hasta özellikleri
Veriler sadece hem tSTART (başlangıç) hem de tEND (sonuç) örnekleri mevcut olduğunda kullanıldı: tEND örnekleri SMOFLipid grubundaki bir hasta için ve ClinOleic grubundaki üç hasta için mevcut değildi. Bu sebeple, iki gruptaki örneklem büyüklüğü sırasıyla 12 ve 16 idi.
Tablo 1. Çalışmayı tamamlayan hastaların özellikleri
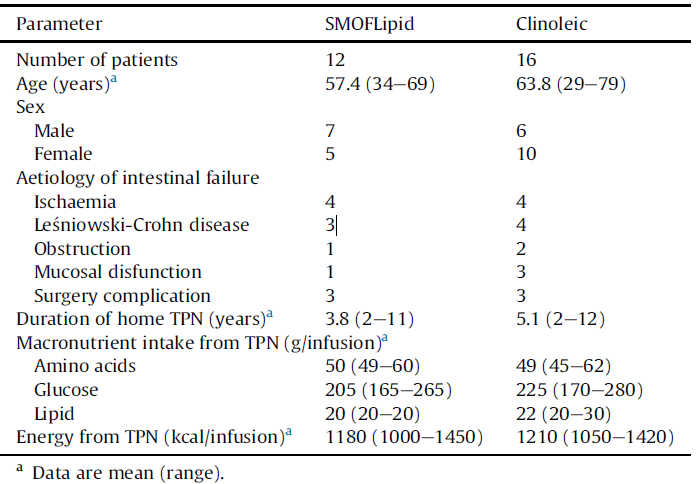
Tablo 1, bu hastaların özelliklerini ve beslenme desteklerinin genel içeriklerini göstermektedir. Hastalar, her gün 16 ila 18 saat boyunca infüze edilen yaklaşık 20 g lipit aldı.
3.2. Değişen lipit emülsiyonunun karaciğer fonksiyonlarının kan belirteçlerine etkisi
Tablo 2. İki tedavi grubunda 60 günlük HPN’nin bir parçası olarak yeni lipid emülsiyonunun (tSTART) öncesinde ve (tEND) sonrasında karaciğer fonksiyon belirteçleri ve kan lipitleri
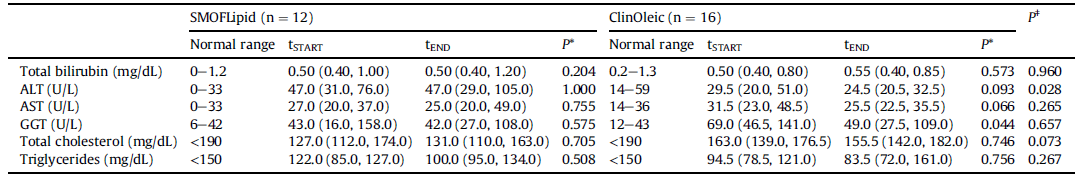
Veriler medyandır (25. percentil, 75. percentil).
p*: Karşılaştırma için P değeri, bir tedavi grubu içinde tSTART’a karşı tEND (Wilcoxon signed ranks testi).
pǂ: tEND grubundaki tedavi grupları arasında karşılaştırma için P değeri (Mann Whitney U-testi).
Ne total bilirubin ne de ölçülen üç karaciğer enzimi (ALT, AST, GGT), hastaların 60 gün boyunca Intralipid’den SMOFLipid’e transferi ile değişmedi (Tablo 2). Total bilirubin, hastaların Intralipid’den ClinOleic’e geçmesiyle de değişmedi (Tablo 2). Bununla birlikte, GGT konsantrasyonu 60 günlük ClinOleic kullanımı sonrasında öncekine göre anlamlı şekilde daha düşüktü (P=0.044; Tablo 2) ve hem ALT hem de AST konsantrasyonları 60 günlük ClinOleic’ten sonra düşme eğilimindeydi (sırasıyla P = 0.093 ve 0.066 ; Tablo 2).
Şekil 1, Her iki tedavi grubu için başlangıçtaki ve sondaki toplam bilirubini ve üç karaciğer enziminin her birini gösterir
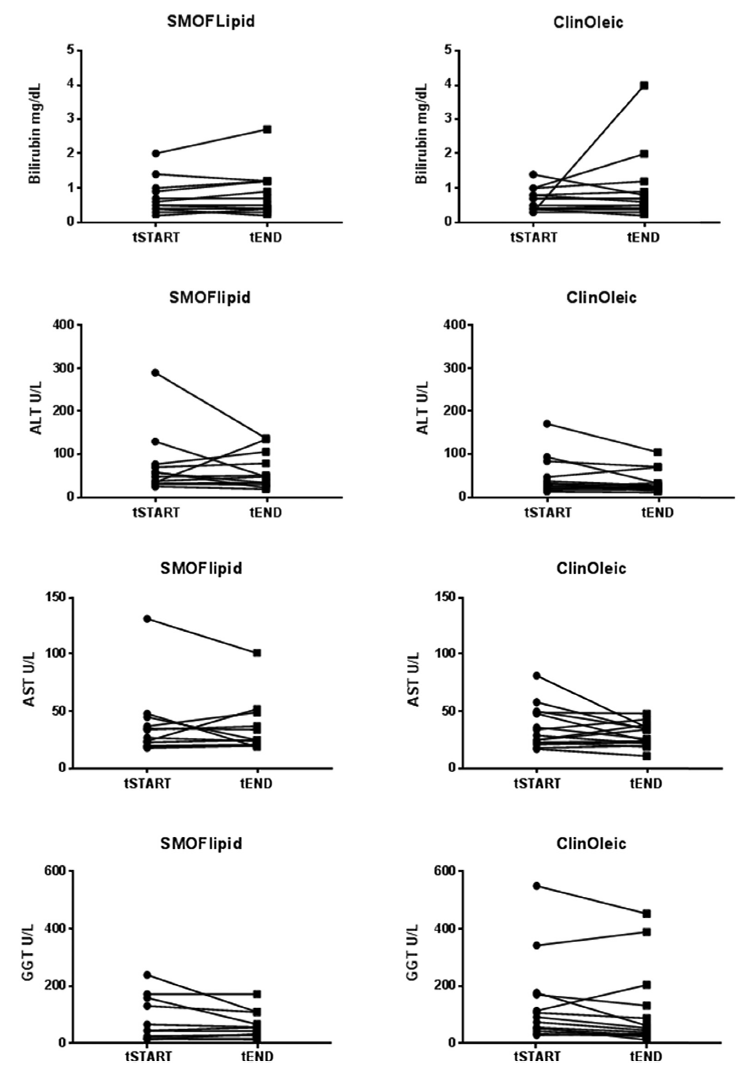
3.3. Değişen lipit emülsiyonunun kan lipit konsantrasyonları üzerine etkisi
60 gün sonrasında iki grup arasındaki plazma total kolesterol ve trigliserit konsantrasyonları SMOFLipid veya ClinOleic tarafından değişmedi (Tablo 2).
3.4.Değişen lipit emülsiyonunun plazma yağ asitleri üzerine etkisi
Tablo 3. İki tedavi grubunda 60 günlük HPN’nin bir parçası olarak yeni lipid emülsiyonunun (tSTART) öncesinde ve (tEND) sonrasında total plazma lipidinin yağ asidi bileşimi (Her bir yağ asidinin total yağ asitlerine yüzdesi verilmiştir)
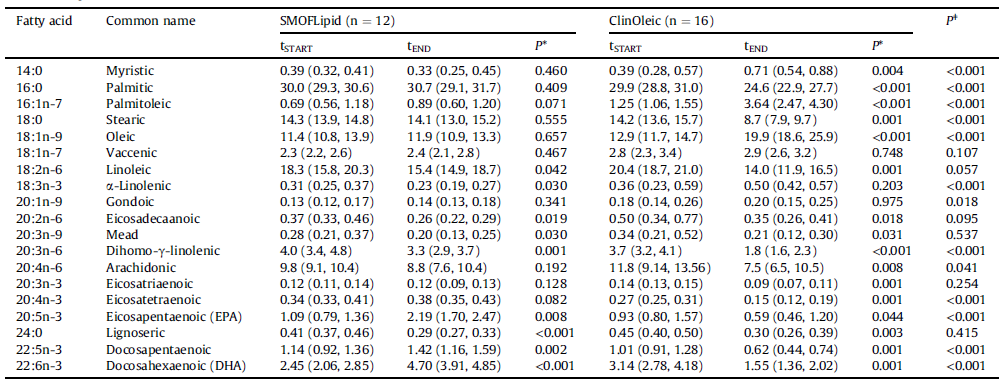
Veriler medyandır (25. percentil, 75. percentil).
p*: Karşılaştırma için P değeri, bir tedavi grubu içinde tSTART’a karşı tEND (Wilcoxon signed ranks testi).
pǂ: tEND grubundaki tedavi grupları arasında karşılaştırma için P değeri (Mann Whitney U-testi).
Toplam plazma lipidinin yağ asidi bileşimi Tablo 3’te gösterilmektedir. Hastaların Intralipid’den SMOFLipid’e transferi; linoleik asit, α-linolenik asit, 20: 2n-6 (linoleik asitin bir uzantısı), dihomo-γ -linolenik asit (20: 3n-6) ve EFA eksikliğinin göstergesi olan mead asit oranlarında önemli düşüşler ile sonuçlanmıştır (Tablo 3). Paralel olarak, EPA ve DHA oranlarında önemli artışlar oldu (Tablo 3). Mead asidinin araşidonik aside oranı anlamlı bir şekilde değişmedi (tSTART: 0.03 (0.02, 0.04)-tEND 0.02 (0.02, 0.03); P = 0.191).
Hastaların Intralipid’den ClinOleic’e transferi ile; palmitik asit (16: 0), stearik asit (18: 0), linoleik asit, 20: 2n-6 (linoleik asidin bir uzantısı), dihomo- γ -linolenik asit (20: 3n-6), EPA ve DHA dahil olmak üzere tüm n-3 PUFA’larda, araşidonik asit, mead asidi oranlarında önemli düşüşlere neden oldu (Tablo 3). Paralel olarak, palmitoleik asit (16: 1n-7) ve oleik asit oranlarında önemli artışlar vardı (Tablo 3). Mead asidinin araşidonik aside oranı anlamlı bir şekilde değişmedi (tSTART: 0.03 (0.02, 0.04)-tEND 0.02 (0.02, 0.04); P = 0.664).
60 günün sonunda (tEND) palmitik asit, stearik asit, dihomo- γ -linolenik asit, araşidonik asit ve hem EPA hem de DHA dahil olmak üzere tüm n-3 PUFA’ların oranları, SMOFLipid grubunda ClinOleic grubundan daha yüksekti. (Tablo 3). Buna karşılık; oleik asit, α- linolenik asit ve 20: 1n-9 (oleik asidin uzantısı) oranları, ClinOleic grubunda SMOFLipid grubundan daha yüksekti (Tablo 3). Mead asidinin araşidonik aside oranı 60 günün sonunda gruplar arasında farklı değildi (P= 0.371).
Genellikle plazma PC’sinde benzer veriler gözlendi (tam veriler gösterilmemiştir). Burada hastaların Intralipid’den SMOFLipid’e transferi EPA’nın (tSTART %0.87 (0.68, 1.00) ve %1.67 (1.10, 2.19); % P= 0.015) ve DHA’nın (tSTART) oranlarını önemli ölçüde arttırdı % 1.35 (1.25, 1.52) vs tEND 2.56 (1.95, 3.04); P= 0.001). Burada hastaların Intralipid’den SMOFLipid’e transferi EPA’nın (tSTART %0.87 (0.68, 1.00) vs. tEND %1.71 (1.10, 2.19); P = 0.015) ve DHA’nın (tSTART %1.35 (1.25, 1.52) ve tEND %2.56 (1.95, 3.04); P = 0.001) oranlarını önemli ölçüde arttırdı. EPA ve DHA’nın oranlarını arttırdı. SMOFLipid grubunda, plazma PC’de mead asidinin araşidonik aside oranlarında önemli bir değişiklik olmamıştır (tSTART 0.03 (0.02, 0.04) ve tEND 0.02 (0.02, 0.03); P = 0.190). ClinOleic grubunda, plazma PC’de mead asidinin araşidonik aside oranlarında anlamlı bir düşüş vardı (tSTART 0.07 (0.05, 0.10) ve tEND 0.04 (0.02, 0.04); P = 0.001).
Hiçbir hastanın plazma total lipitlerinde veya plazma PC’sinde mead asidin araşidonik aside oranı > 0.2 üzerine geçmemiştir; plazma toplam lipidinde ve plazma PC’de en yüksek oranlar sırasıyla 0.05 ve 0.19’du.
Tablo 4. İki tedavi grubunda 60 günlük HPN’nin bir parçası olarak yeni lipid emülsiyonunun (tSTART) öncesinde ve (tEND) sonrasında sitokinlerin plazma konsantrasyonları (pg / ml).
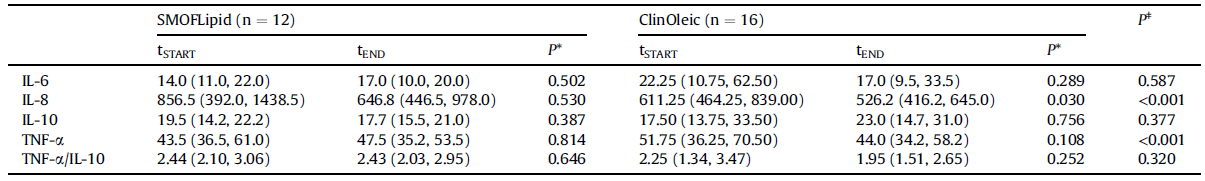
Veriler medyandır (25. percentil, 75. percentil).
p*: Karşılaştırma için P değeri, bir tedavi grubu içinde tSTART’a karşı tEND (Wilcoxon signed ranks testi).
pǂ: tEND grubundaki tedavi grupları arasında karşılaştırma için P değeri (Mann Whitney U-testi).
3.5. Değişen lipit emülsiyonunun plazma sitokin konsantrasyonları üzerine etkisi
IL-1 β, IL-12 ve IFN- γ konsantrasyonları, plazma örneklerinin çoğunda tespit sınırının altındaydı. Buna karşılık, IL-6, IL 8, IL10 ve TNF- α, bütün numunelerde kolayca tespit edildi ve bu dört sitokin konsantrasyonları, Tablo 4’te rapor edildi. TNF- α’nın IL-10’a oranı da (Tablo 4) bir “enflamatuar indeks” olarak rapor edilir, çünkü TNF-α pro-enflamatuardır ve IL-10 anti-enflamatuardır ve ikisi birbirinin hareketlerine antagonist hareket eder. IL-6, IL-10 ve TNF- α konsantrasyonları ve TNF- α’nın IL-10’a oranı, SMOFLipid veya ClinOleic’e transfer olmuş olunsa da değişmedi (Tablo 4). Hastalar 60 gün boyunca ClinOleic aldıklarında IL-8 konsantrasyonu azaldı ve bu durumda konsantrasyon SMOFLipid grubundan daha da düşük oldu (Tablo 4).
4. TARTIŞMA
HPN, beslenme gereksinimlerini uzun süre oral veya enteral yolla karşılayamayan hastalarda yetersiz beslenmeyi önlemeyi amaçlar [1-3]. Lipid emülsiyonları; yağ asidi kaynağı olarak esansiyel yağ asitlerinden linoleik asidi ve α-linolenik asidi içeren PN formülasyonlarının temel bileşenlerindendir. HPN’de kullanılan geleneksel lipit emülsiyonları, soya fasulyesi yağına dayanır ve EFA’lar, özellikle linoleik asit bakımından zengindir. Daha düşük bir linoleik asit içeriğine sahip olan yeni lipit emülsiyonları geliştirilmiştir. Çünkü soya fasulyesi yağının, linoleik asit fazlalığına sebep olduğu endişesi vardır. Soya fasulyesi yağında fazla olan bu esansiyel yağ asidinin sebep olabileceği endişeler arasında karaciğer hastalığı ve enflamasyon vardır [4,11,16]. Bu çalışmada, yetişkinlerin uzun vadeli HPN için soya yağı bazlı bir lipit emülsiyonundan, 8 hafta boyunca iki yeni lipit emülsiyonundan birine aktarılmasının etkisi karşılaştırılmıştır. Kullanılan yeni lipit emülsiyonları: 80:20 zeytinyağı ve soya fasulyesi yağı karışımı olan ClinOleic ve 30: 30: 25: 15 soya yağı, orta zincirli trigliseritten zengin yağ, zeytinyağı ve balık yağı karışımı olan SMOFLipid idi. ClinOleic, oleik asit bakımından zengindir; SMOFLipid, biyoaktif uzun zincirli n-3 PUFA’lar EPA ve DHA sağlar. Hem ClinOleic hem de SMOFLipid, karaciğer hastalığını-riskini ve iltihaplanmayı azaltabilir. Bununla birlikte, bu lipid emülsiyonlarının her ikisi de EFA’lar açısından soya fasulyesi yağının içeriğinden daha fakir olması, EFA eksikliğine neden olabilecekleri konusunda bir endişeye sebep olmuştur. Bu nedenle, bu çalışmada EFA eksikliği belirteci de dahil olmak üzere karaciğer fonksiyon, inflamasyon ve yağ asidi durumu ölçülmüştür. Her iki lipit emülsiyonunun, plazmanın yağ asidi profilinde belirgin değişikliklere neden olduğu, ancak EFA eksikliğine dair kanıt bulunmadığı tespit edildi. Bununla birlikte, yağ asitlerindeki değişikliklere rağmen, SMOFLipid karaciğer fonksiyon belirteçlerini, kan lipitlerini veya plazma sitokinlerini değiştirmemişken ClinOleic; dört karaciğer fonksiyon marköründen birini (GGT) ve üç sitokinden birini (IL-8) ılımlı ölçüde azaltan etkilere sahipti.
Plazmanın (ve PC bileşeninin) yağ asidi bileşiminde gözlenen değişiklikler, farklı lipit emülsiyonlarının bileşimi ile tutarlıdır. Yetişkin HPN’de Intralipid yerine yedek olarak SMOFLipid veya ClinOleic kullanılmasının, kandaki linoleik asit miktarını azaltacağı konusunda net kanıtlar mevcuttur. Ayrıca, n-6 linoleik asit türevlerinde de bir düşüş vardır. Paralel olarak, ClinOleic oleik asidi arttırırken, SMOFLipid EPA ve DHA’yı arttırır. ClinOleic ve SMOFLipid’in yağ asidi profilleri üzerindeki bu etkileri, erişkin hastalarda HPN üzerine yapılmış olan sınırlı literatür ile tutarlıdır [17-20]. ClinOleic ve SMOFLipid’in oleik, linoleik, α- linolenik ve araşidonik asitler, EPA ve DHA üzerindeki gözlenen etkileri çeşitli pediatrik ve yetişkin hasta gruplarında bildirilenlerle tutarlıdır [21].
İlginç bir şekilde, hem ClinOleic hem de SMOFLipid’de sağlanan EFA’ların miktarı Intralipid’den çok daha az olmasına rağmen (Giriş’e bakınız) her ikisinin de müdahalenin öncesinde ve sonunda tüm hastalarda mead / araşidonik asit oranını değiştirmediği, plazmadaki mead asit oranında küçük bir azalmayla sonuçlandığı gözlemlendi. Müdahalenin öncesinde ve sonunda bu oran tüm hastalarda <0.2 idi. Son gözlem; ne SMOFLipid ne de ClinOleic’in, HPN’de yetişkinlerde EFA eksikliğini indüklemeyeceğini göstermektedir. Bu, yetişkin HPN hastalarında ClinOleic’in kullanımı hakkındaki sınırlı verilerle tutarlıdır [17,18,20]. Bulgular, hem ClinOleic hem de SMOFLipid’de sağlanan linoleik ve α-linolenik asitlerin miktarının, bu hasta grubundaki EFA gereksinimini karşılamak için yeterli olduğunu göstermektedir.
Intralipid’in uzun süre kullanılmasının, bağırsak yetmezliği ile ilişkili karaciğer hastalığı olarak adlandırılan karaciğer hastalığını desteklediği düşünülmektedir. Bu, n-6 PUFA’ların fazla içerdiğinden veya fitosterollerin varlığından dolayı olabilir [5]. Hem ClinOleic hem de SMOFLipid, Intralipid’den çok daha düşük miktarda n-6 PUFA içerir (bkz. Giriş). SMOFLipid, Intralipid’den daha az fitosterol içerir. Fitosterol kompozisyonu farklı olmasına rağmen total miktar Intralipid ve ClinOleic arasında benzerdir [22]. SMOFLipid, Intralipid’e göre avantajlar sunabilir, çünkü EPA ve DHA hepatik lipid metabolizmasını ve iltihabını modüle edebilir [4]. Balık yağı içeren lipit emülsiyonlarının, özellikle pediatrik hastalarda [23] ayrıca yetişkinlerde de bağırsak yetmezliği ile ilişkili karaciğer hastalığını önlediği hem de iyileştirdiği gösterilmiştir [24]. Bu çalışmada SMOFLipid; hastaların Intralipid aldığı zamana kıyasla karaciğer fonksiyon belirteçlerini değiştirmedi, ClinOleic ise GGT seviyelerini düşürdü. Önceki çalışmalar; ClinOleic’in HPN alan erişkin hastalarda karaciğer fonksiyon belirteçleri üzerindeki etkisinin çok az olduğunu ortaya koydu [17,18]; Bu çalışmada ClinOleic’in total bilirubin, AST ve ALT üzerinde etkisinin olmaması, bununla tutarlıdır. SMOFLipid’in HPN alan erişkinlerde bilirubin, ALT ve AST’yi düşürdüğü gösterilmiştir [19]. Son yapılan çalışma, mevcut çalışmaya göre daha kısa sürdü (4 hafta-8 hafta arası) ancak daha büyüktü. Bununla birlikte, bu çalışmada karaciğer fonksiyon belirteçleri için tEND ve tSTART verilerinin benzerliği, küçük örneklem büyüklüğü nedeniyle etki olmadığını göstermektedir. Bu nedenle, bu çalışmada SMOFLipid’in neden karaciğer fonksiyon belirteçlerini iyileştirmediği net değildir. Enflamasyon üzerindeki etkisinin olmamasıyla ilişkili olabilir (aşağıya bakınız). EPA ve DHA sağlayan lipit emülsiyonlarının, HPN alan yetişkin hastalarda bağırsak yetmezliği ile ilişkili karaciğer hastalığının tedavi sürecinde fayda sağlayıp sağlayamayacağını doğrulamak için bu alanda daha fazla araştırma yapılması gerekmektedir.
N-3 PUFA’ların (EPA ve DHA), örnek sistemlerde bariz bir şekilde anti-enflamatuar özellikler gösterdikleri belirtilmiştir [25]. Ayrıca oleik asit biraz anti-enflamatuar aktiviteye sahip olabilir [8-9]. EPA ve DHA içeren LE’lerin kullanılmasının; ameliyattan sonra, kritik hastalıklarda, bazı enflamatuar belirteçlerin kan konsantrasyonlarını düşürdüğü gösterilmiştir [16]. Bu gibi hastanede yatan hastalarda ClinOleic ile yapılan sınırlı sayıda çalışma, enflamatuar belirteçler üzerinde bir etkisi olmadığını bildirmiştir [16]. Yetişkin HPN hastalarında yapılan çalışmalar, ClinOleic [17-18] veya SMOFLipid’in [19] kanda enflamasyon belirteçleri üzerinde bir etkisi olmadığını bildirmiştir. Bu nedenle, SMOFLipid’in iltihaplanma üzerindeki etkisi ve bu çalışmada ClinOleic’in görülen sınırlı etkisi, yapılmış az sayıdaki literatürle tutarlıdır.
Mevcut çalışmanın bir sınırlaması, hastaların aldıkları lipide rastgele atanmamış olmasıdır. Ek olarak, sadece bir tek zaman noktası değerlendirildi (8 hafta). Lipit değerlerindeki değişikliklerin zaman sürecini araştırmak da önemli olabilir. Bu bağlamda, önceden yapılmış bir çalışma [19], 4 hafta sonra SMOFLipid’in HPN alan yetişkinlerde bilirubin, ALT ve AST’yi düşürdüğünü bildirdi.
5. SONUÇ
Hem SMOFLipid hem de ClinOleic, daha önce Intralipid kullanan yetişkin HPN hastalarında plazmanın yağ asidi profilini önemli ölçüde değiştirir. Lipid emülsiyonu bu hastalarda EFA eksikliğine neden olmaz. SMOFLipid karaciğer fonksiyon belirteçlerini veya iltihabını değiştirmedi. Buna karşılık, ClinOleic, hepsi olmasa da bazı karaciğer fonksiyon ve inflamasyon belirteçlerini azalttı. SMOFLipid ve ClinOleic, yetişkin HPN hastalarında kullanım için düşünülebilir.
Fon Kaynakları
Bu araştırma; kamu, ticari veya kar amacı gütmeyen sektörlerdeki finansman kuruluşlardan herhangi bir özel hibe almamıştır.
Yazarlık beyanı
SO, çalışmayı tasarladı ve genel yönetiminden sorumluydu. MK, JS, MO ve MR, çalışmaya dahil edilecek hastaları tanımladı. SO, MK ve JS müdahaleyi gerçekleştirdi. JT ve KM, lipid emülsiyonlarını değiştirme prosedürünü denetlemekten sorumluydu ve kan numunelerini aldı. HLF, PCC gözetimi altında yağ asidi ve sitokin konsantrasyonlarını belirledi. HLF ve PCC istatistiksel analiz yaptı. PCC makaleyi hazırladı. Tüm yazarlar makalenin son halini onayladı.
Çıkar çatışması beyannamesi
SO, MK, JS, JT, KM, MO, MR ve HLF’lerin herhangi bir çıkar çatışması yoktur. PCC; Fresenius-Kabi, B. Braun Melsungen ve Baxter Healthcare’e danışmanlık yapmaktadır.
Ek veriler
Bu makale ile ilgili ek veriler aşağıdaki adreste bulunabilir:
https://doi.org/10.1016/j.clnu.2018.05.028
0261-5614/© 2018 Published by Elsevier Ltd
ALT, alanin aminotransferaz;
AST, aspartat aminotransferaz;
DHA, dokosaheksaenoik asit;
EFA, esansiyel yağ asidi;
EPA, eikosapentaenoik asit;
GGT, gama-glutamiltranspeptidaz;
HPN, evde parenteral beslenme;
IFN, interferon;
IL, interlökin;
LE, lipit emülsiyonu;
PC, fosfatidilkolin;
PN, parenteral beslenme;
PUFA, çoklu doymamış yağ asidi;
TNF, tümör nekroz faktörü.
[2] Staun M, Pironi L, Bozzetti F, Baxter J, Forbes A, Joly F, et al. ESPEN guidelines on parenteral nutrition: home parenteral nutrition (HPN) in adult patients. Clin Nutr 2009; 28:467-79.
[3] Pironi L, Arends J, Bozzetti F, Cuerda C, Gillanders L, Jeppesen PB, et al. ESPEN guidelines on chronic intestinal failure in adults. Clin Nutr 2016;35: 247-307.
[4] Calder PC, Adolph M, Deutz NE, Grau T, Innes JK, Klek S, et al. Lipids in the intensive care unit: recommendations from the ESPEN expert group. Clin Nutr 2018 Feb;37(1):1-18.
[5] Beath SV, Kelly DA. Total parenteral nutrition-induced cholestasis: prevntion and management. Clin Liver Dis 2016; 20:159-76.
[6] Baker EJ, Miles EA, Burdge GC, Yaqoob P, Calder PC. Metabolism and functional effects of plant-derived omega-3 fatty acids in humans. Prog Lipid Res 2016; 64:30-56.
[7] Calder PC. Functional roles of fatty acids and their effects on human health. J Parenter Enter Nutr 2015;39(1 Suppl.):18S-32S.
[8] Calder PC. Marine omega-3 fatty acids and inflammatory processes: effects, mechanisms and clinical relevance. Biochim Biophys Acta 2015; 1851:469-84.
[9] Calder PC. Omega-3 fatty acids and inflammatory processes: from molecules to man. Biochem Soc Trans 2017; 45:1105-15.
[10] Vangaveti VN, Jansen H, Kennedy RL, Malabu UH. Hydroxyoctadecadienoic acids: oxidised derivatives of linoleic acid and their role in inflammation associated with metabolic syndrome and cancer. Eur J Pharmacol 2016; 785:70-6.
[11] Pironi L, Agostini F, Guidetti M. Intravenous lipids in home parenteral nutrition. World Rev Nutr Diet 2015; 112:141e9.
[12] Holman RT. Essential fatty acid deficiency. Prog Lipid Res 1968; 9:275e348.
[13] Holman RT. The ratio of trienoic:tetraenoic acids in tissue lipids as a measure of essential fatty acid requirement. J Nutr 1960; 70:405-10.
[14] Jones CJ, Calder PC. Influence of different intravenous lipid emulsions on fatty acid status and laboratory and clinical outcomes in adult patients receiving home parenteral nutrition: a systematic Review. Clin Nutr 2018 Feb;37(1):285-91.
[15] Browning LM, Walker CG, Mander AP, West AL, Madden J, Gambell JM, et al. Incorporation of eicosapentaenoic and docosahexaenoic acids into lipid pools when given as supplements providing doses equivalent to typical intakes of oily fish. Am J Clin Nutr 2012; 96:748-58.
[16] Calder PC. Lipids for intravenous nutrition in hospitalised adult patients: a multiple choice of options. Proc Nutr Soc 2013; 72:263-76.
[17] Reimund JM, Rahmi G, Escalin G, Pinna G, Finck G, Muller CD, et al. Efficacy and safety of an olive oil-based intravenous fat emulsion in adult patients on home parenteral nutrition. Aliment Pharmacol Ther 2005; 21:445-54.
[18] Vahedi K, Atlan P, Joly F, Le Brun A, Evard D, Perennec V, et al. A 3-month double-blind randomised study comparing an olive oil- with a soyabean oilbased intravenous lipid emulsion in home parenteral nutrition patients. Br J Nutr 2005; 94:909-16.
[19] Klek S, Chambrier C, Singer P, Rubin M, Bowling T, Staun M, et al. Four-week parenteral nutrition using a third generation lipid emulsion (SMOFlipid) e a double-blind, randomised, multicentre study in adults. Clin Nutr 2013;32: 224-31.
[20] Olthof ED, Roelofs HM, Fisk HL, Calder PC, Wanten GJ. No clinical or biochemical evidence for essential fatty acid deficiency in home patients who depend on long-term mixed olive oil- and soybean oil-based parenteral nutrition. J Parenter Enteral Nutr 2016; 40:982-8.
[21] Dai YJ, Sun LL, Li MY, Ding CL, Su YC, Sun LJ, et al. Comparison of formulas based on lipid emulsions of olive oil, soybean oil, or several oils for parenteral nutrition: a systematic review and meta-analysis. Adv Nutr 2016; 7:279-86.
[22] Savini S, D’Ascenzo R, Biagetti C, Serpentini G, Pompilio A, Bartoli A, et al. The effect of 5 intravenous lipid emulsions on plasma phytosterols in preterm infants receiving parenteral nutrition: a randomized clinical trial. Am J Clin Nutr 2013; 98:312-8.
[23] Nandivada P, Fell GL, Gura KM, Puder M. Lipid emulsions in the treatment and prevention of parenteral nutrition-associated liver disease in infants and children. Am J Clin Nutr 2016; 103:629S-34S.
[24] Burns DL, Gill BM. Reversal of parenteral nutrition-associated liver disease with a fish oil-based lipid emulsion (Omegaven) in an adult dependent on home parenteral nutrition. J Parenter Enteral Nutr 2013; 37:274-80.
[25] Sales-Campos H, Souza PR, Peghini BC, da Silva JS, Cardoso CR. An overview of the modulatory effects of oleic acid in health and disease. Mini Rev Med Chem 2013; 13:201-10.



![Evde Parenteral Beslenen Yetişkinlerde Lipid Bileşeni Değişiminin Etkisi [Çeviri]](https://www.birbes.com/wp-content/uploads/2019/10/Evde-Parenteral-Beslenen-Yetişkinlerde-Lipid-Bileşenleri-Değişiminin-Etkisi-750x375.png)


![Evde Parenteral Nutrisyona Bağımlı Yetişkinlerde İhtiyaç Temelli Yaşam Kalitesi [Çeviri]](https://www.birbes.com/wp-content/uploads/2019/10/Evde-Parenteral-Nutrisyona-Bağımlı-Yetişkinlerde-İhtiyaç-Temelli-Yaşam-Kalitesi-350x250.jpg)
![Total Parenteral Nütrisyon (TPN) Alan Yetişkinlerde Refeeding Sendromu: Üçüncü Basamak Tedavi Merkezinde Kapsamlı Bir İnceleme (İngiltere) [Çeviri]](https://www.birbes.com/wp-content/uploads/2019/10/Total-Parenteral-Nütrisyon-TPN-Alan-Yetişkinlerde-Refeeding-Sendromu-Üçüncü-Basamak-Tedavi-Merkezinde-Kapsamlı-Bir-İnceleme-İngiltere-Çeviri-350x250.png)
![Erkek Basketbolcularda Düşük Karbonhidratlı Diyetin Ardından, Yedi Gün Boyunca Uygulanan Karbonhidrat Yüklemesi Sonrası Anaerobik Performans [Çeviri]](https://www.birbes.com/wp-content/uploads/2019/10/Erkek-Basketbolcularda-Düşük-Karbonhidratlı-Diyetin-LCD-Ardından-7-Gün-Boyunca-Uygulanan-Karbonhidrat-Yüklemesi-Sonrası-Anaerobik-Performans-350x250.jpg)


